通过多途径输注4次干细胞,脊髓损伤患者运动评分提升798.2%,功能独立性显著提高
来源: 发布日期:2026-01-20 浏览次数:681次
近期,《World Journal of Stem Cells》发表了一篇关于干细胞治疗完全性脊髓损伤I期临床试验研究成果,文献显示,参与者输注4次干细胞后1年,功能独立性、运动功能、ASIA评分均得到显著改善,其中ASIA运动评分较基线平均提升798.2%(从1.67到15.0)。

创伤性脊髓损伤(SCI)是最严重的疾病之一,它会破坏感觉和运动通路,导致永久性残疾和长期并发症,从而损害多个器官的功能。
SCI病理生理机制复杂,可分为两个既有区别又相互关联的阶段:初级阶段,以机械性创伤为特征,导致即刻的轴突和神经元损伤;次级阶段,以兴奋性毒性、氧化应激、炎症和凋亡等一系列事件为特征,进一步加重了最初的损伤。
尽管急性期治疗取得了显著进展,包括早期手术减压和康复治疗,但这些干预措施主要侧重于提高生存率和减轻损伤过程,而非从根源上恢复神经功能。鉴于这些局限性,迫切需要针对SCI急性期和慢性期的新型治疗方法。
有研究发现,脂肪组织和牙髓来源的MSCs能改善啮齿动物SCI模型的运动功能并缩小病灶面积,提示MSCs在促进脊髓修复方面可能发挥重要作用。此外,我们之前研究也证实了脐带来源MSCs(UC-MSCs)在治疗包括SCI在内多种神经系统疾病方面的安全性和可行性。
目 的:这些发现为目前I期临床试验奠定了基础,该试验旨在评估通过多种途径输注UC-MSCs在慢性完全性SCI患者中的安全性和初步疗效。
患者资料:该研究共纳入6例患者,年龄19-39岁,男5例,女1例,损伤原因包括交通事故、摔伤、枪伤和滑雪事故,损伤部位包括T5-12的爆裂性骨折,损伤持续时间6个月-12年。
移植前过程:用于输注的UC-MSCs来自3代培养的细胞,被重悬于生理盐水中,浓度分别为3ml中含1*10⁶个细胞(鞘内注射)、20ml中含1*10⁶个细胞(肌内注射)以及30ml中含1*10⁶个细胞(静脉注射)。
方 法:每个患者在每个治疗周期(每月给药2次,持续2个月)均同时采用三种给药途径,术后患者在重症监护室观察1天,然后转至神经外科进行后续的物理治疗和康复,并在每次输注前后重复上述方案。
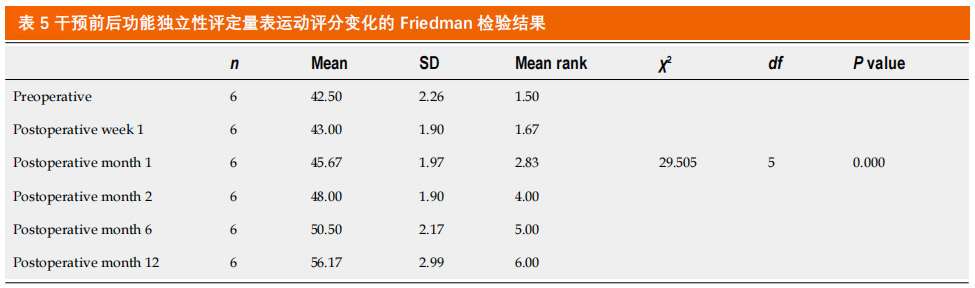
功能独立性改善:第1周FIM运动评分未观察到显著变化,在随后的几个月均观察到持续显著改善(表5),表明该干预措施对运动功能恢复具有长期益处。与术前相比,术后12个月FIM运动评分提升32.16%。
痉挛程度改善:右和左下肢痉挛程度在第1周内未观察到明显变化,在随后的几个月中,痉挛程度得到了显著且持续的改善(表6、7)。与术前相比,术后12个月Ashworth评分提升72.88%和72.29%。
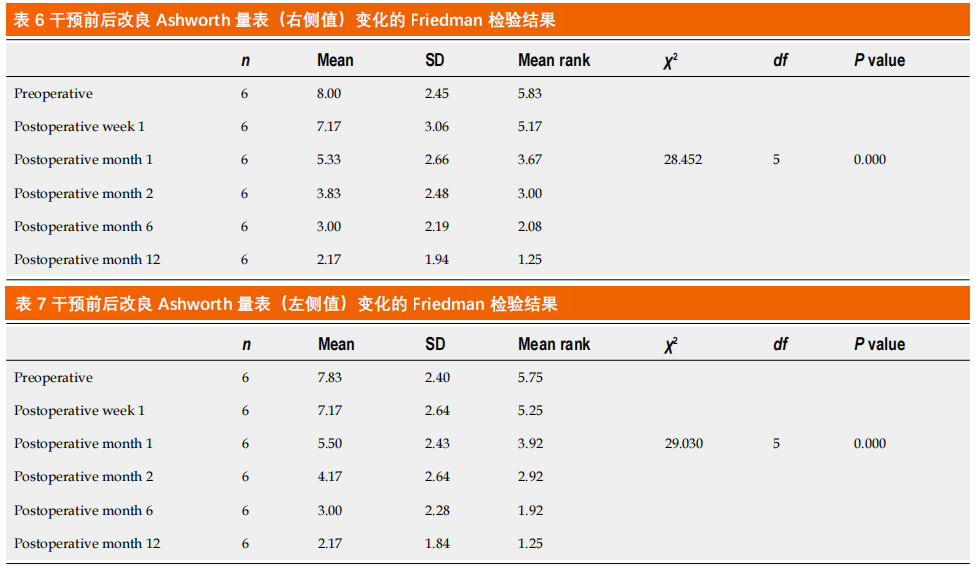
虽然痉挛程度的降低不是立即出现,但随着时间推移,痉挛程度呈现出显著且渐进的下降趋势,这表明该治疗对运动功能恢复有显著效果。
ASIA运动评分:第1周和1个月时,ASIA运动评分均无显著变化,2个月时首次检测到运动功能显著改善,4个月时观察到进一步显著改善,并在1年随访中持续改善(表8)。与术前相比,术后12个月ASIA运动评分较基线提升798.2%(从1.67到15.0)。
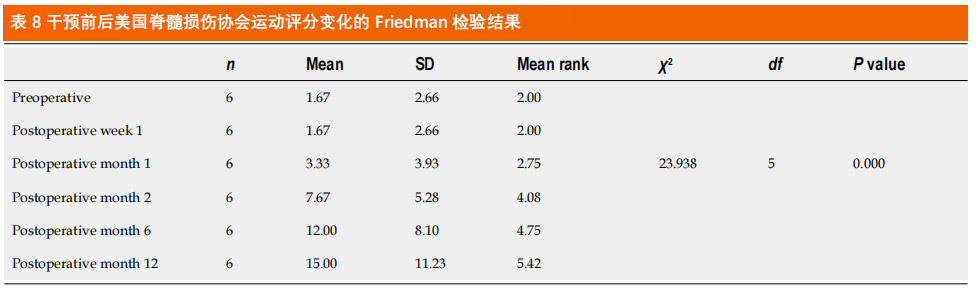
这些结果表明,该治疗虽然即时效果并不明显,但干预的益处会随着时间推移显著且持续地改善运动功能。
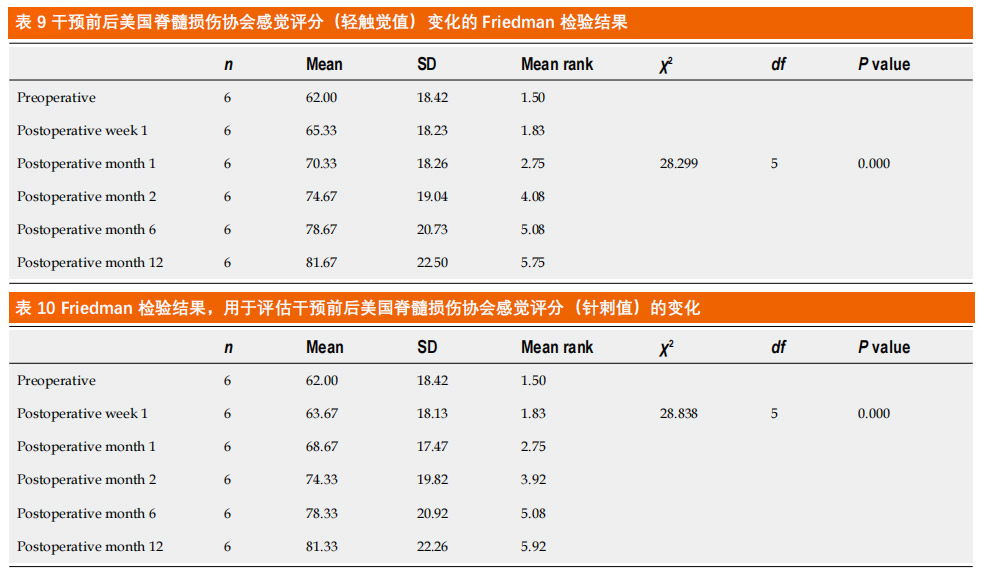
ASIA感觉评分:干预后评估显示,轻触(LT)和针刺痛(PP)两种感官评分,从术后1周到随访结束均有显著改善(表9、10),与术前相比,术后12个月LT和PP分别提升31.73%和31.18%。这反映出随时间推移感觉功能得到显著提高。
安全性结果:在为期1年的随访期间,没有报告重大安全问题或不良事件,没有发生严重感染、与麻醉相关并发症、过敏反应或休克事件。此外,也未观察到神经功能恶化或SCI进展的迹象。
总 结:该项研究结果表明,完全性SCI患者在接受UC-MSCs治疗后,运动和感觉功能显著改善,同时痉挛减轻,生活质量提升,这些发现支持了UC-MSCs疗法作为SCI一种有前景的治疗选择。
参考资料:
Kaplan N, Kabatas S, Civelek E, Savrunlu EC, Akkoc T, Boyalı O, Öztürk E, Can H, Genc A, Karaöz E. Multiroute administration of Wharton's jelly mesenchymal stem cells in chronic complete spinal cord injury: A phase I safety and feasibility study. World J Stem Cells 2025; 17(5): 101675.10.4252/wjsc.v17.i5.101675.
















