自体骨髓谱系阴性细胞治疗RP:12个月随访,56.7%患者视功能显著改善,病程短者获益更佳!
来源: 发布日期:2026-04-29 浏览次数:6次
近期,国际期刊《Stem Cells International》刊发一项临床研究,证实自体骨髓源性谱系阴性(Lin⁻)细胞玻璃体内注射治疗视网膜色素变性(RP),可安全稳定改善患者视功能。

RP是临床最常见遗传性视网膜变性疾病,全球患病率约1/4000,核心病理为周边视杆细胞进行性损伤,先引发夜盲与周边视野缩窄,随病情进展累及黄斑,最终导致中心视力下降、色觉异常,晚期可发展为完全失明。
目前已发现超200个基因、3000余种突变可引发RP,遗传方式与基因型直接决定发病年龄和进展速度。视网膜高代谢状态、氧化应激、局部血流下降、小胶质细胞激活等因素,会共同加速感光细胞凋亡,形成不可逆视功能损伤。
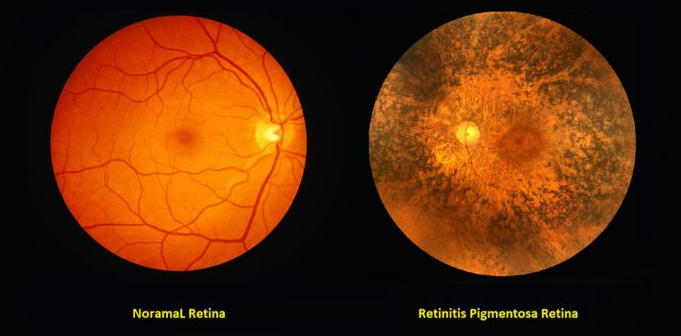
传统干预手段中,大剂量维生素 A、叶黄素、DHA 等营养补充,无法显著改善患者视网膜功能。维生素E摄入甚至会加速ERG振幅下降,抗炎药物与基因疗法虽安全性尚可,但整体疗效有限,神经保护成为该病治疗的核心研究方向。
临床前研究已证实,Lin⁻细胞玻璃体内注射可在视网膜损伤模型中,显著提升局部BDNF表达水平,能有效整合入视网膜各层,精准挽救受损感光细胞,为后续人体临床试验奠定了扎实的理论与实践基础。
患者筛选:本研究为单中心、前瞻性、开放标签非随机临床试验,共纳入30例RP患者,女12例、男18例,平均年龄41.72±12.77岁,排除其它眼病、全身病及近期相关治疗干预。
细胞来源和剂量:入组患者均接受自体骨髓后髂嵴穿刺取材,在GMP标准实验室完成 Lin⁻细胞分离与纯化。所有患者均接受玻璃体内单次注射,剂量1×10⁶个细胞。
评估指标:研究设置多维度评估指标,包括最佳矫正远视力、对比敏感度、眼压、视网膜 OCT、静态视野、多焦 ERG、全视野ERG、PERG及生活质量评分,随访12个月。
视力改善情况:术后12个月,治疗眼最佳矫正视力呈现显著提升趋势(表2),56.7%患者视力得到改善。病程<10年患者获益更显著,平均提升14个字母(表3),远优于病程>10年患者,提示早期干预可大幅提升治疗效果。
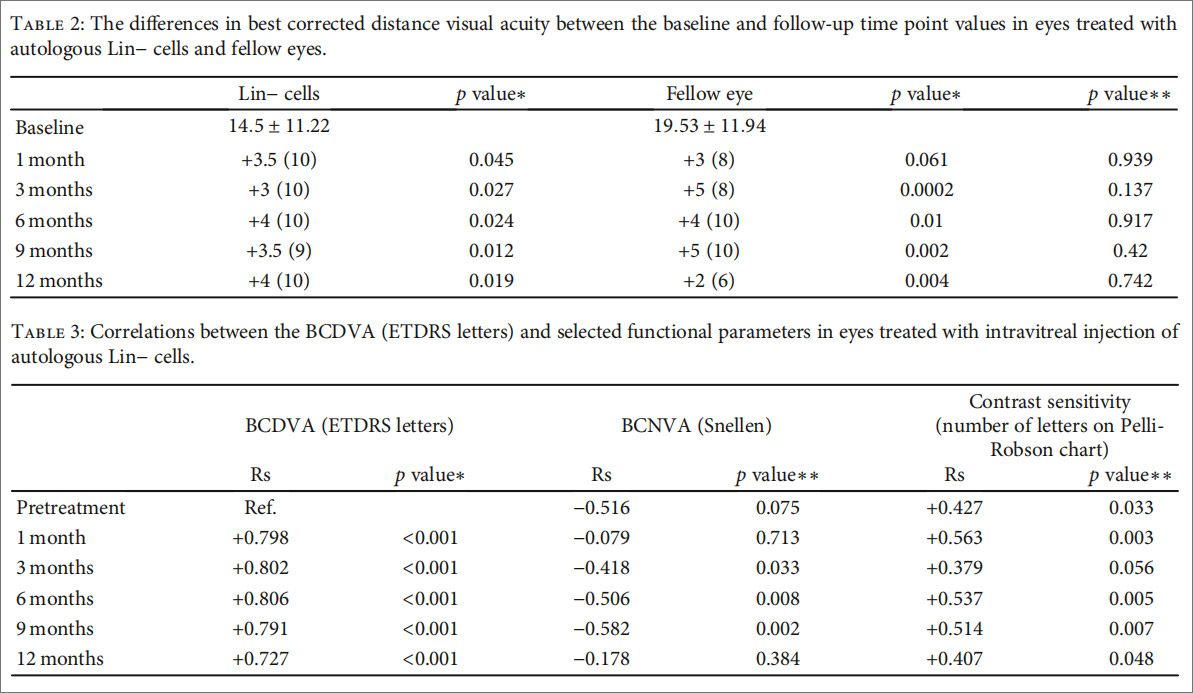
亚组分析结果揭示,基线黄斑形态对治疗疗效影响显著,黄斑水肿程度越轻,患者术后视力提升越明显。正常黄斑与黄斑萎缩患者无显著相关性,提示无明显水肿的患者更易从治疗中获益。
多焦电生理检查结果:术后治疗眼中心10°区域P1波反应密度(表4),在所有随访时间节点均显著高于对侧对照眼。中心凹视锥细胞功能得到稳定保护,而对照眼呈自然衰退趋势,证实细胞疗法具有靶向保护作用。
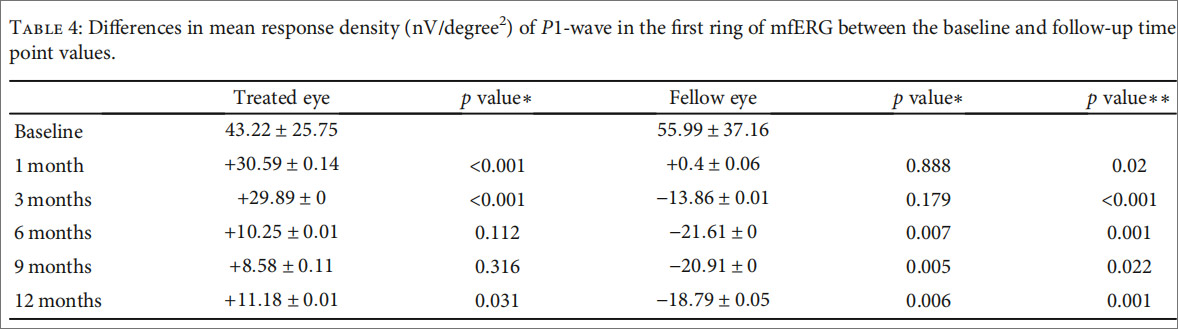
视野改善情况:10-2 静态视野检测数据表明,治疗眼平均偏差在术后12个月显著改善,且明显优于对侧对照眼。30-2视野无显著差异,提示Lin⁻细胞对中心视野的保护作用更明确,与视锥细胞营养支持机制高度契合。
生活质量评分:术后6-9个月该评分显著提升,评分变化与视野改善程度呈正相关。患者对病程进展主观感知越慢,生活质量评分越高,证实该治疗可同时改善客观视功能与主观生活体验。
代表性结果:见图1。
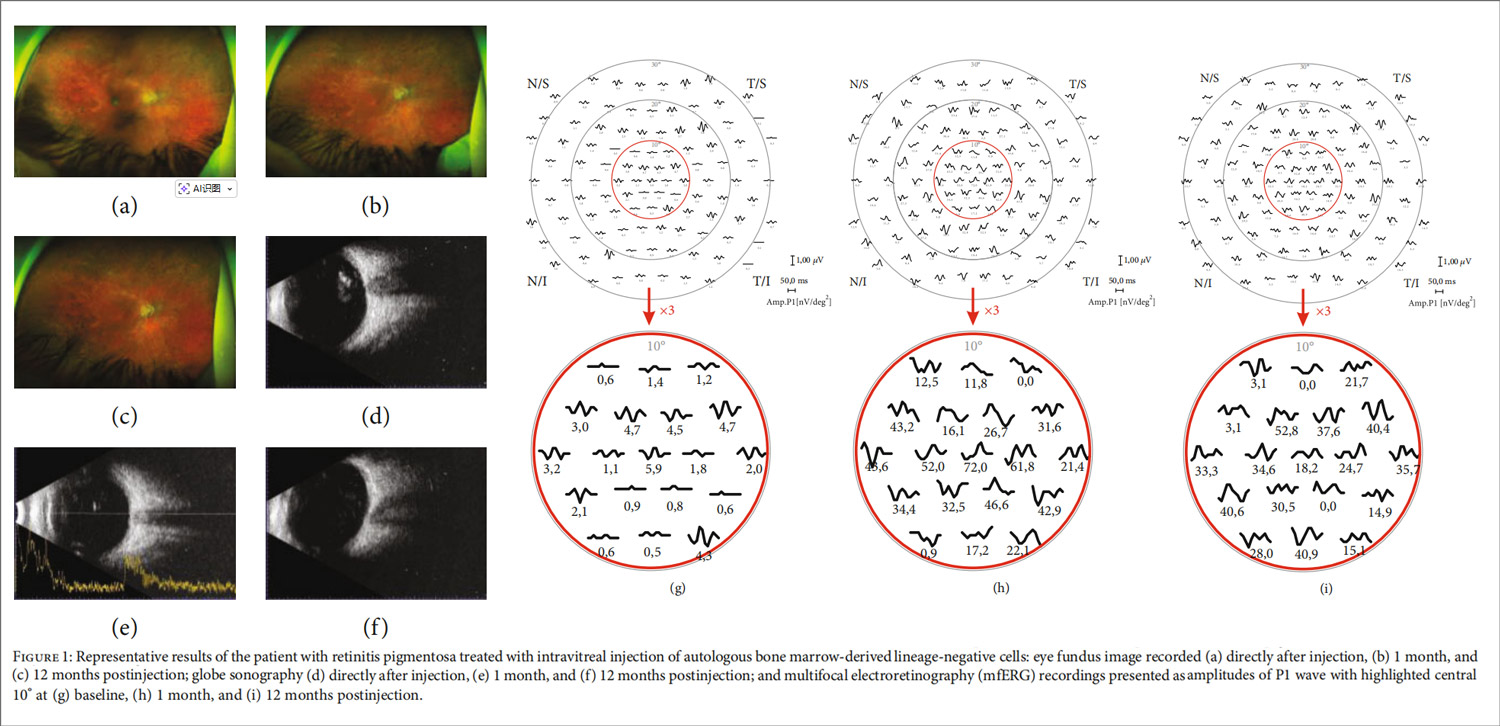
安全性分析:随访显示,该疗法整体耐受性良好,仅3例患者出现牵拉性视网膜脱离,经玻璃体切割手术治疗后完全复位,未造成永久视功能损伤。无明显眼内炎症、眼压失控等严重不良事件发生。
该研究是全球首个大样本自体骨髓 Lin⁻细胞治疗RP长期临床研究,证实玻璃体内注射方式安全可行,通过神经营养与抗炎双重机制,稳定视锥细胞功能,延缓疾病进展。
与其它干细胞给药途径相比,玻璃体内注射可直接突破血视网膜屏障,让细胞精准作用于病变区域。自体细胞无免疫排斥风险,无需使用免疫抑制剂,细胞特性更易渗透至视网膜深层发挥作用。
研究虽存在非随机、单中心等局限性,但自身对照设计有效排除自然病程干扰,12个月持续获益的临床数据,为临床转化提供强力支撑,也为后续剂量优化、重复治疗提供明确方向。
综上所述,自体骨髓源性Lin⁻细胞玻璃体内注射治疗RP安全有效,可持续改善患者中心视力、视野与电生理指标。病程早期、黄斑结构完好的患者获益最为显著,有望成为临床标准化干预方案。
未来需开展多中心、随机对照试验,进一步优化细胞剂量与注射频次,长期评估疗效与安全性。推动这一创新细胞疗法从科研走向临床,为更多RP患者带来重获光明的希望。
参考资料:
Marta P. Wiącek et al.Long-Term Effects of Adjuvant Intravitreal Treatment with Autologous Bone Marrow-Derived Lineage-Negative Cells in Retinitis Pigmentosa.Stem Cells International Volume 2021, Article ID 6631921, 12 pages.10.1155/2021/6631921.















