好消息!NK细胞体外扩增关键瓶颈获得突破!
来源: 发布日期:2026-04-02 浏览次数:573次
近日,深圳市一五零生命科技有限公司联合深圳市第三人民医院科研团队,通过构建“腺病毒+ NK细胞”双阶段疗法,借助肿瘤微环境“自饲养(self-feeder)”效应,显著提升NK细胞对实体瘤的控制,突破单一疗法局限,实现体外扩增与原位激活高效协同,有效解决NK细胞治疗核心瓶颈。该成果发表在《Cellular Immunology》。

癌症作为全球重大公共卫生威胁,传统治疗手段难以攻克实体瘤的免疫抑制屏障。自然杀伤细胞(NK细胞)是先天抗肿瘤免疫核心效应细胞,却因肿瘤浸润不足、活性受限、微环境抑制等问题,难以发挥稳定疗效。
一、NK细胞治疗实体瘤核心困境
NK细胞是机体抗肿瘤免疫第一道防线,可精准识别并清除MHC-I分子缺失的肿瘤细胞,无需抗原致敏便能快速杀伤。但实体瘤患者体内NK细胞常出现数量减少、功能耗竭,且难以穿透致密肿瘤基质,加上免疫抑制因子作用,其归巢、活化与存活能力显著降低。
体外扩增是提升NK细胞数量的关键,基于K562饲养细胞的扩增体系已成为临床主流,需外源添加细胞因子以促进NK增殖,存在培养周期长、细胞易衰老等问题。优化扩增方案、提升体内活性,是NK细胞临床转化关键。
二、工程化饲养高效扩增NK细胞
为实现NK细胞高效体外扩增,研究团队构建了能同时表达IL-2、膜结合型IL-21和4-1BBL工程化K562饲养细胞(图1)。经γ射线灭活后,该细胞可稳定分泌细胞因子,14天内使NK细胞扩增超100倍、纯度超85%,且扩增出的NK细胞活化程度高、杀伤能力显著增强。
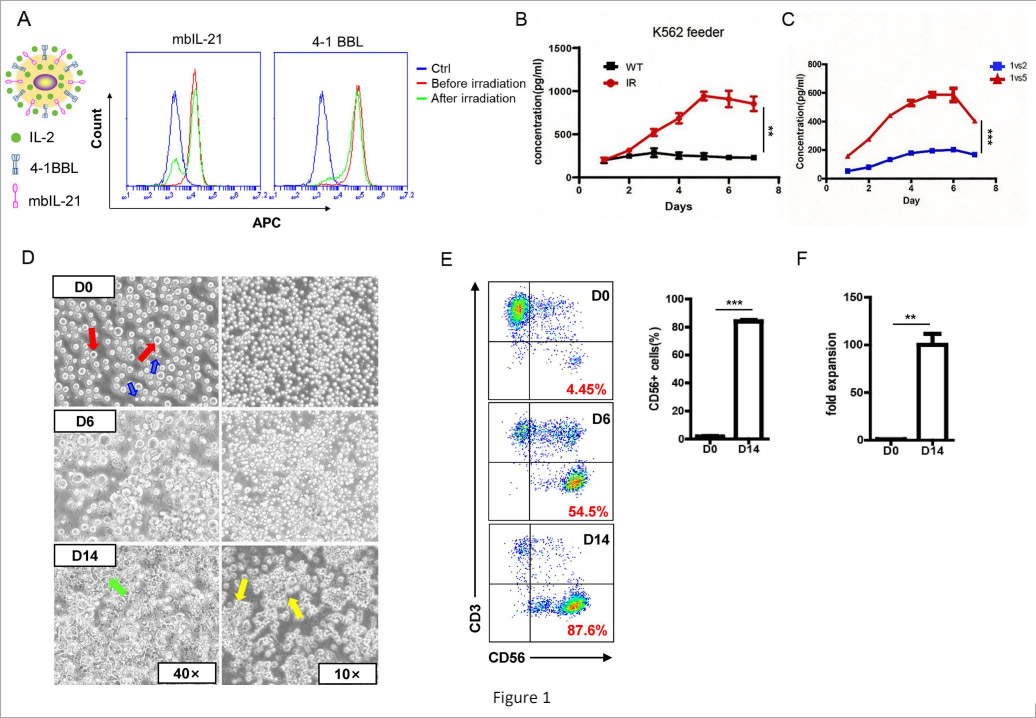
与传统体系相比,该改良饲养细胞无需额外添加大量因子,既缩短培养周期、减少细胞衰老,又保留了NK细胞抗肿瘤活性(图2)。
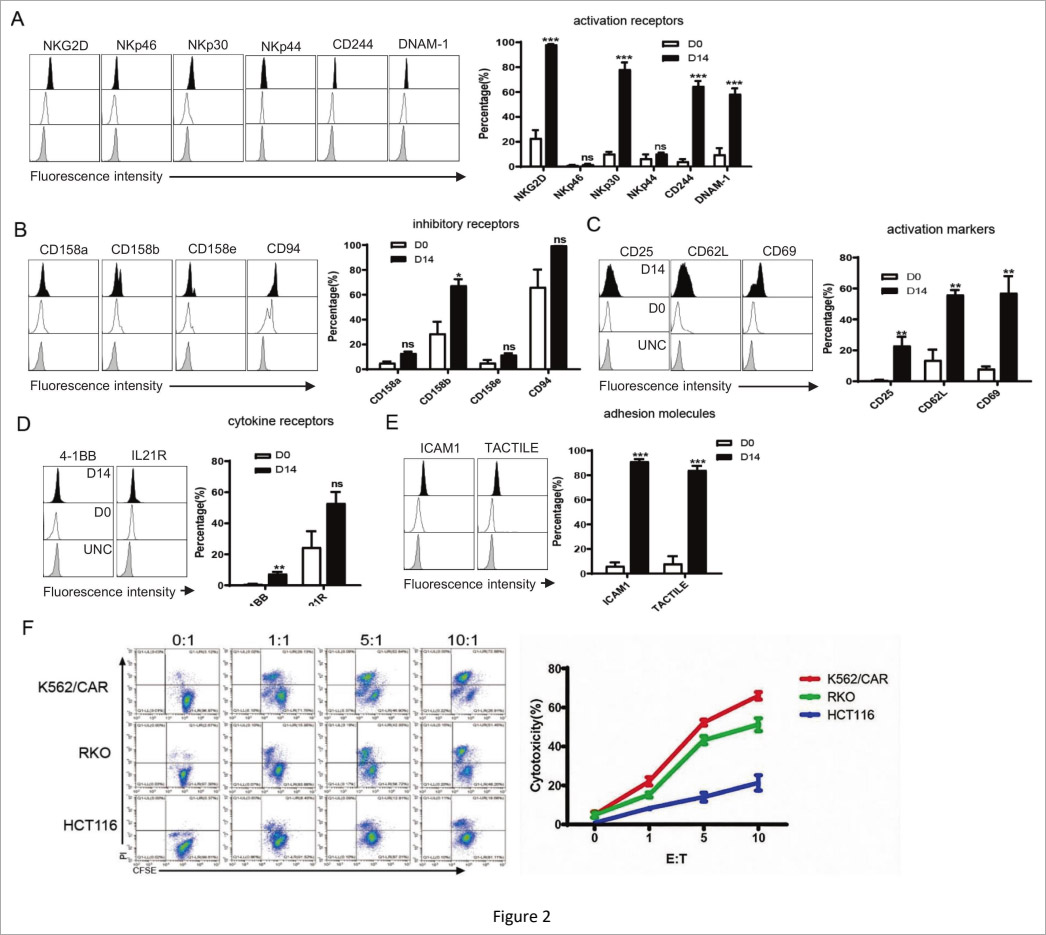
扩增后的NK细胞高表达多种活化受体,黏附与细胞因子受体也同步上调,肿瘤识别、浸润及杀伤能力更强,为体内输注奠定坚实基础。
三、腺病毒重塑肿瘤免疫微环境
研究发现,腺病毒可在肿瘤内选择性复制、裂解癌细胞并激活免疫,是重塑肿瘤微环境理想载体,也为解决NK细胞体内活化与存活问题提供了新方向。
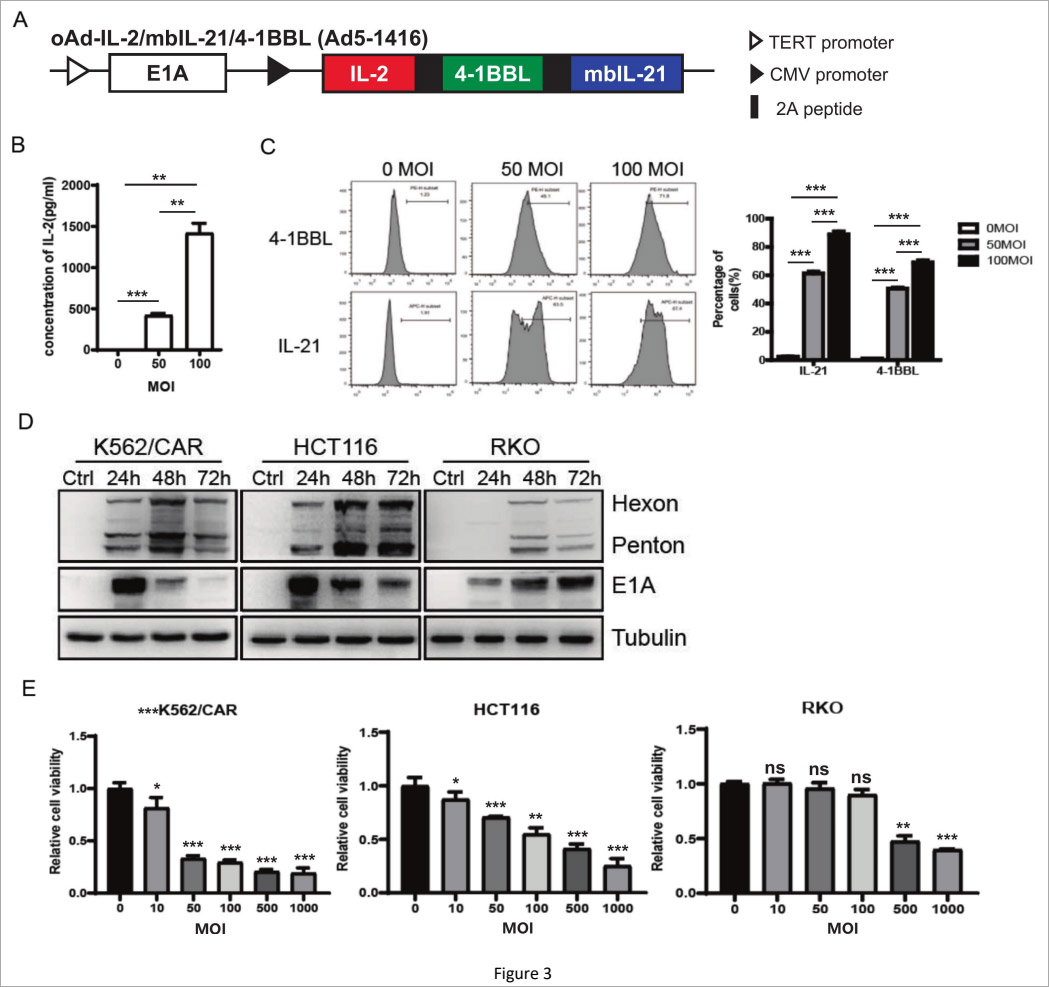
研究团队构建的重组溶瘤腺病毒能靶向肿瘤复制裂解(图3),可将肿瘤转化为免疫因子工厂,持续释放免疫调节分子,重塑免疫微环境。该腺病毒以人端粒酶启动子调控复制,优先在肿瘤细胞内选择性复制,对正常细胞影响极小,兼具靶向溶瘤与免疫调节双重功能,从根源降低治疗副作用。
四、携带溶瘤功能的腺病毒体内外实验
体外实验证实,该腺病毒可在K562、HCT116等肿瘤细胞内高效复制,发挥显著溶瘤效应。同时,病毒表达的免疫因子能强力促进NK细胞增殖、活化与迁移,提升IFN-γ分泌水平,增强NK细胞对肿瘤细胞裂解能力,展现出良好的体外协同作用(图4)。
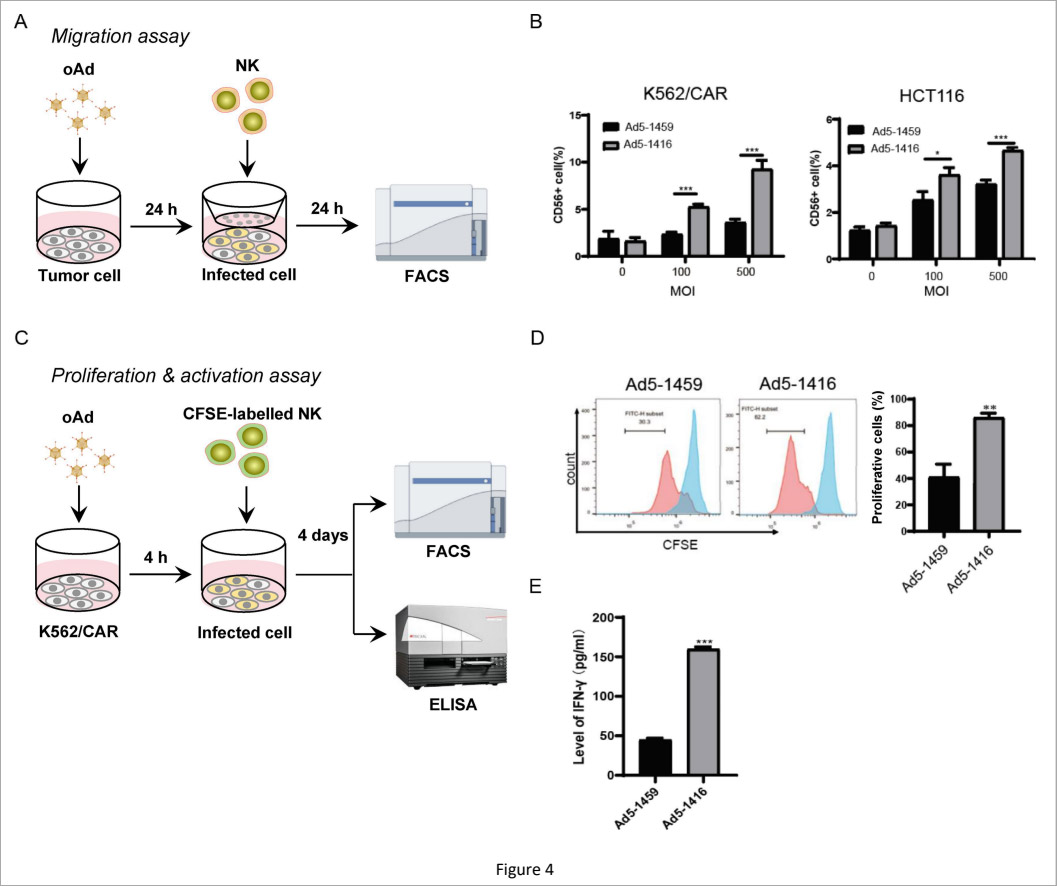
此外,该病毒可在肿瘤局部构建“自饲养”效应:受感染的肿瘤细胞模拟工程化K562饲养细胞功能,持续为浸润NK细胞提供增殖与活化信号,形成独立免疫刺激环路,克服肿瘤微环境的免疫抑制,维持NK细胞长期活性。
为验证体内治疗效果(图5),研究团队构建HCT116结直肠癌皮下荷瘤小鼠模型,采用瘤内注射携带溶瘤功能的腺病毒联合静脉输注扩增NK细胞治疗方案。
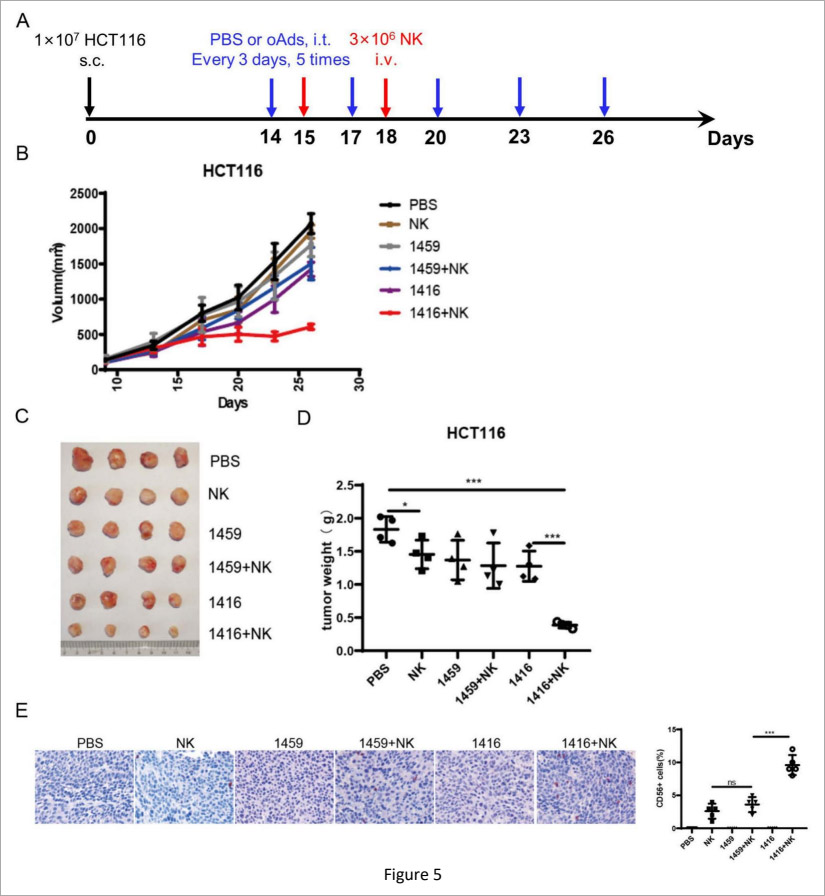
结果显示,单一病毒或NK细胞治疗仅能轻度抑制肿瘤,而联合组肿瘤生长显著受控,肿瘤重量大幅降低。
免疫组化结果证实,联合治疗组肿瘤组织中CD56+NK细胞浸润量显著提升,远高于单一治疗组。这表明携带溶瘤功能的腺病毒不仅直接裂解肿瘤细胞,更通过“自饲养”效应招募并激活NK细胞,形成更强的协同抗肿瘤作用,实现1+1>2的治疗效果。
五、联合治疗破解实体瘤三大难题
从作用机制来看,该联合策略精准突破NK细胞治疗实体瘤三大难题:一是通过体外扩增解决NK细胞数量不足;二是借助携带溶瘤功能的腺病毒提升NK细胞肿瘤归巢与浸润效率;三是利用“自饲养”效应维持NK细胞在肿瘤微环境中的活性与增殖能力(图6)。
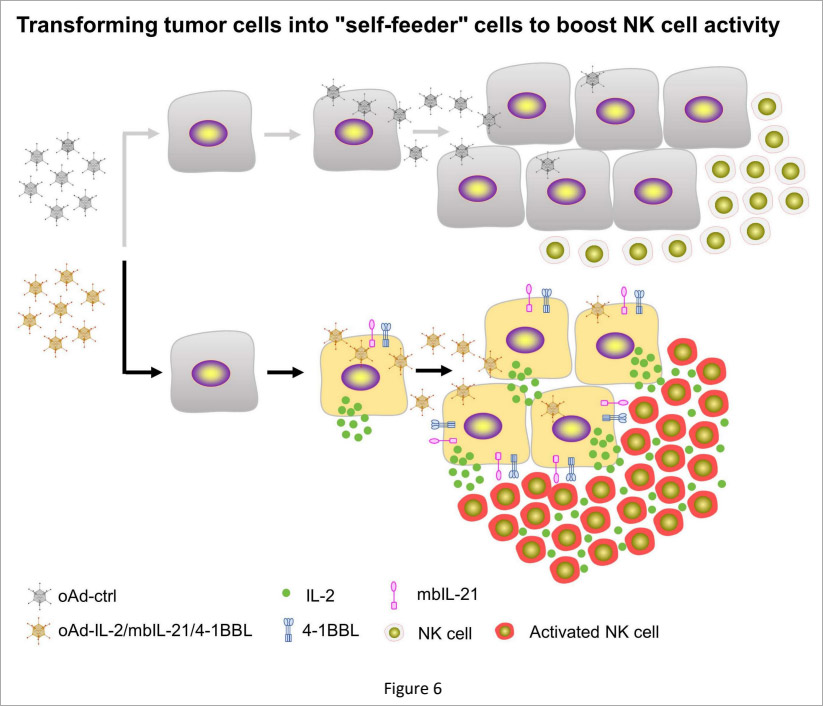
与传统全身给予细胞因子的方案相比,携带溶瘤功能的腺病毒能大幅降低全身毒性,同时实现靶向免疫激活。该策略不依赖患者自身免疫状态,对免疫功能低下实体瘤患者同样适用,具备广泛临床适配性。
六、临床前景与未来研究方向
目前该研究仍存在一定局限,如采用免疫缺陷小鼠模型,无法完全模拟人体免疫清除作用;深部实体瘤的瘤内注射存在临床操作挑战;NK细胞长期存活与记忆样功能仍需优化。但这些问题均指向明确研究方向,为后续研究提供了清晰路径。
未来可通过导入IL-12、IL-15等基因进一步升级携带溶瘤功能的腺病毒,借助间充质干细胞(MSC)等载体实现病毒精准递送,同时完善给药时机与剂量方案,推动该策略从基础研究走向临床转化。
综上所述,携带溶瘤功能的腺病毒联合NK细胞,通过体外扩增与原位激活双管齐下,重塑实体瘤免疫微环境,突破传统NK细胞疗法核心局限。该方案兼具靶向性、安全性与高效性,为结直肠癌等实体瘤提供了极具潜力免疫治疗新策略。
这一研究不仅验证了携带溶瘤功能的腺病毒与细胞免疫联合治疗的巨大潜力,更提出“自饲养”免疫激活新理念,为后续实体瘤免疫治疗研发提供重要理论与技术支撑。随着研究不断深入,该策略有望走向临床,为广大实体瘤患者带来全新治疗选择与长期生存希望。
参考资料:
Qibin Liao, Siqiang Lai, Zhongyi Fan, Ning Li, Bo Zou, Mingshu Han, Yuanzheng Peng, Junchang Wu, Jing Xun, Xiaohua Tan.Armed oncolytic adenovirus elicits a “self-feeder” effect to supercharge NK cells for solid tumor control.Cellular Immunology Available online 29 March 2026, 105100.10.1016/j.cellimm.2026.105100.















