干细胞治疗间质性膀胱炎6个月:67%患者病灶缩小/完全消失,夜尿频率显著下降
来源: 发布日期:2025-08-18 浏览次数:2147次
导 读:间质性膀胱炎(IC)是一种慢性、致残性疾病,现有有效治疗选择有限。首次人体临床试验结果显示,一种干细胞疗法在难治性间质性膀胱炎(IC)患者中展现出良好的安全性和疗效,不仅减轻了临床症状,还在Hunner病灶中诱导了结构性改善。这些发现为IC患者提供了一种新的治疗策略。
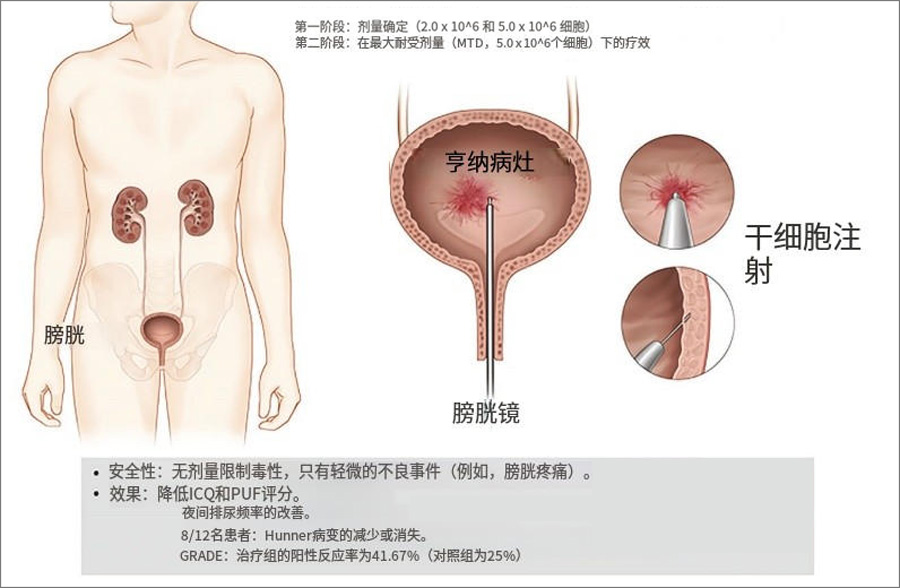
IC是一种慢性泌尿系统疾病,主要特征为盆腔疼痛、尿急、尿频及夜尿症等,显著影响患者生活质量。IC分为Hunner型(特征性膀胱溃疡)和非Hunner型,前者约占10%,但症状更严重。
流行病学数据显示,IC全球患病率约为0.1%-0.5%,男女患病比例差异明显,女性发病率是男性5-10倍,高发年龄为40-60岁。有研究表明,约30% IC患者对常规治疗无反应,其中Hunner型患者预后更差。
IC发病机制尚未完全阐明,目前认为与以下因素相关:
● 上皮屏障缺陷:膀胱黏膜层的糖胺聚糖(GAG)缺失导致尿液成分渗透,引发炎症;
● 神经源性炎症:感觉神经异常激活释放P物质,加剧疼痛和尿急;
● 自身免疫反应:部分患者体内检测到抗膀胱抗体;
● IC病变类型:Hunner型病变常伴随肥大细胞浸润和纤维化,提示局部组织修复障碍。
在生理层面,IC造成的慢性疼痛会导致睡眠障碍和性功能障碍,长期尿频还可能引发肾功能损伤;在心理社会层面,约60%患者合并焦虑或抑郁,社会功能显著下降;在经济负担层面,Hunner型患者因症状顽固,更易发展为膀胱挛缩,需手术干预,增加治疗费用。
现有IC治疗方案(包括口服药物/膀胱灌注/神经刺激/尿道电灼术等)只能暂时性缓解症状,不仅高复发率,患者还会长期受疼痛困扰。亟需开发能针对IC病理机制的新型疗法,实现根本性治疗。
近年来,干细胞疗法成为再生医学领域一种极具前景的治疗途径,其中间充质干细胞(MSCs)因其免疫调节和再生修复潜力成为了IC治疗突破点。临床前研究表明,MSCs可通过分泌生长因子(如VEGF、IGF-1)促进膀胱血管生成和上皮再生,并抑制Th1/Th17介导的炎症反应。
近日,《Stem Cells Translational Medicine》期刊报道了一项IC临床试验,文献显示,12例患者经MR-MC-01(一种来源于人胚胎干细胞的MSCs疗法)治疗后6个月,夜间排尿频率显著下降,8例病变减轻/完全消失(67%),5例(41.67%)整体反应评分显示中等/显著改善。

患者筛选:共纳入22例受试者(平均年龄>60岁),其中I期6例(5女1男),IIa期16例(11女5男)。IIa期16例受试者中,12例分配至MR-MC-01组,4例分配至安慰剂组,两组共有6例受试者中途退出,均非因不良反应而退出。
干预方法:通过膀胱镜引导,然后在Hunner病灶周围的膀胱壁20个部位进行黏膜下注射MR-MC-01,安慰剂组以相同方式注射等量生理盐水,每位受试者注射总量为10ml。
I期试验中,3名受试者接受低剂量细胞(2.0*107)治疗,3名受试者接受高剂量细胞(5.0*107)治疗。高剂量被确定为最大耐受剂量(MTD),并在IIa期中使用(见图1),12名受试者中8名接受MR-MC-01治疗,4名受试者接受安慰剂治疗。
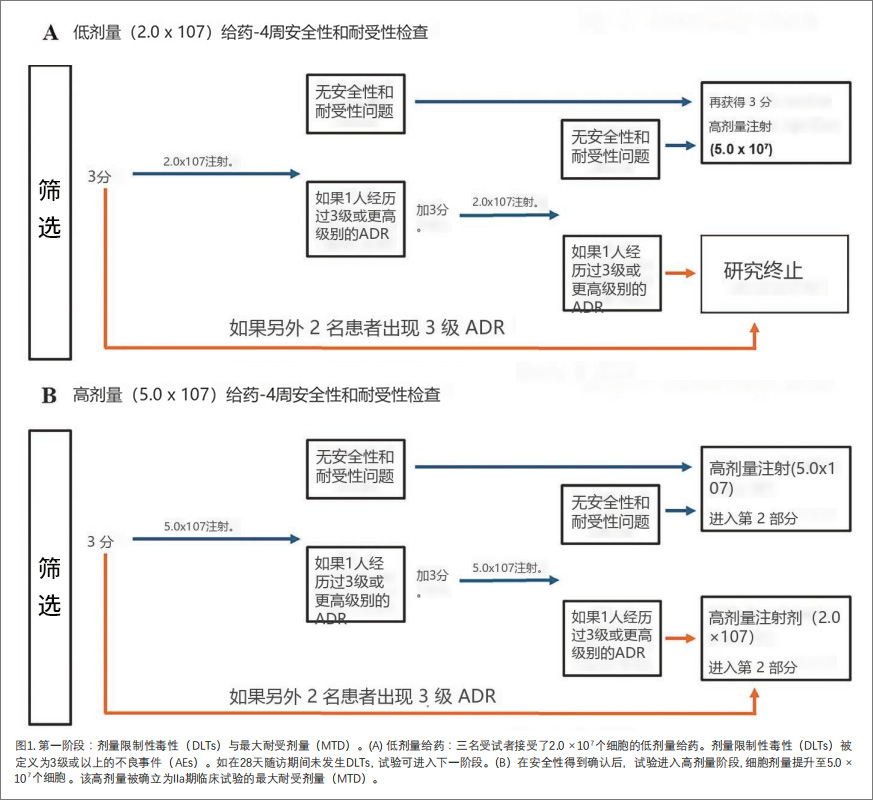
安全性结果:I期研究中,未观察到剂量限制性毒性(DLTs),最常见不良事件(AEs)为轻度膀胱疼痛及操作不适,均自愈。IIa期研究中,MR-MC-01组报告5例治疗相关轻度AEs,无严重AEs。
临床评估结果:6个月随访显示,MR-MC-01组ICQ(间质性膀胱炎问卷)评分降低5.50±6.93分(安慰剂3.00±7.35),PUF(盆腔疼痛及尿急/尿频)评分降低4.75±5.53分(安慰剂2.25±4.43),两组差异显著(图3A,B),证实其对IC症状的改善明显优于安慰剂。
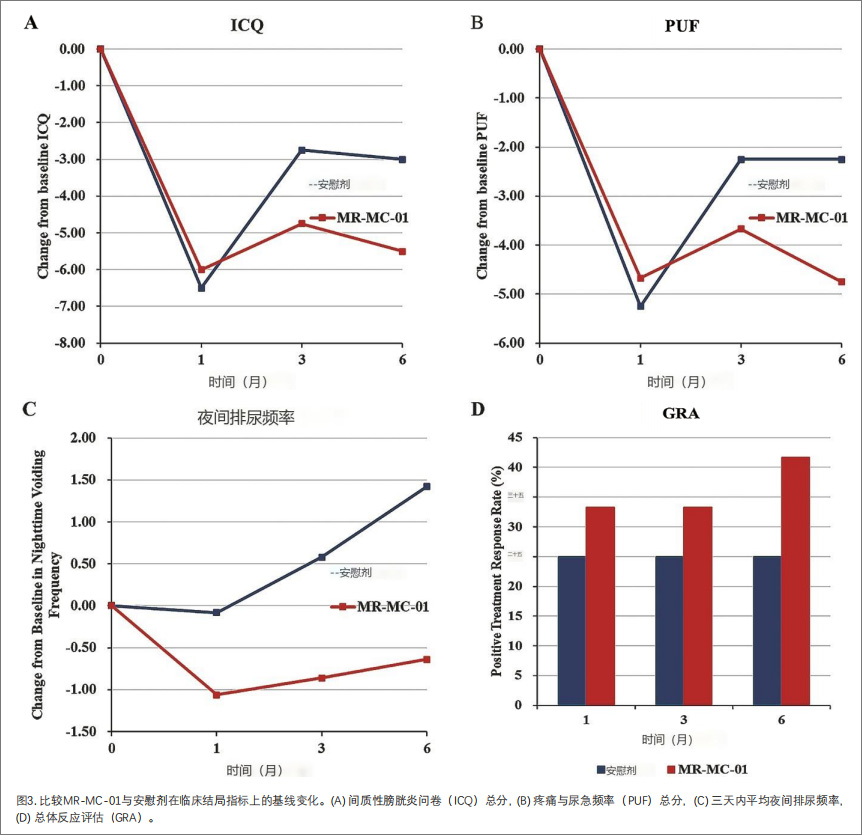
夜间排尿频率:3个月和6个月时,MR-MC-01组患者夜间排尿频率均显著下降。6个月时,MR-MC-01组夜间排尿次数平均减少0.64 ± 1.20次,而安慰剂组则平均增加1.42 ± 1.10次。夜间尿频减少表明膀胱功能得到显著改善,有助于提升患者生活质量(图3C)。
整体反应评估:6个月时,MR-MC-01组中有41.67%患者报告了中度到显著改善,对照组仅为25%。这种改善提示MR-MC-01可能为IC患者提供显著的症状缓解益处,特别是对常规治疗反应不佳患者(图3D)。
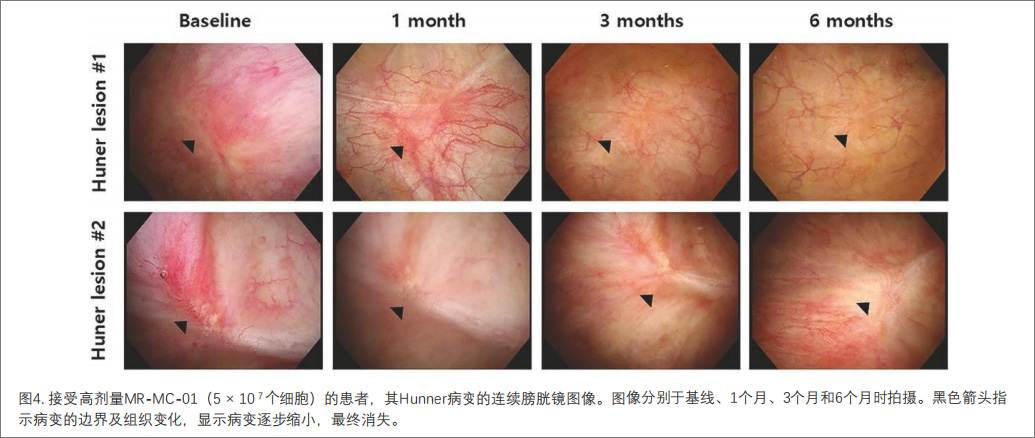
膀胱镜检查结果:6个月时,MR-MC-01组12名患者中有8名Hunner病变减轻/完全消失,而安慰剂组未见显著变化。这提示MR-MC-01可能促进IC患者膀胱病变的愈合或缓解,显示出该方案的潜在疗效优势(图4)。
总 结:上述研究结果表明,MR-MC-01是一种安全且有效的治疗手段,对已无其它治疗选择的IC患者具有显著潜力。本研究突出了其在缓解症状和改善生活质量方面的优势,安全性与疗效数据均表现良好。
未来研究应深入探讨其作用机制,并开展更大规模、多中心的临床试验,以进一步验证上述发现并优化治疗方案。
参考资料:
Yoon Soo Kyung et al.A single-center, phase 1/2a trial of hESC-derived mesenchymal stem cells (MR-MC-01) for safety and efficacy in interstitial cystitis patients.Stem Cells Translational Medicine, 2025, 14, szaf018,10.1093/stcltm/szaf018 Advance access publication 19 May 2025.