静脉输注两疗程干细胞:10例SPMS患者病灶数量/体积显著减少,残疾和心理状态明显改善
来源: 发布日期:2026-04-10 浏览次数:7次
近日,《Stem Cell Research & Therapy》刊发了一项I/IIa期临床试验结果,证实静脉输注自体脂肪间充质干细胞(AT-MSC),可安全改善继发进展型多发性硬化症(SPMS)患者的残疾状态、神经功能与生活质量,为难治性SPMS提供再生治疗新方向。
多发性硬化症(MS)是中枢神经系统慢性自身免疫性脱髓鞘疾病,以轴突变性、神经修复不足为核心病理,会导致不可逆残疾。约80%复发缓解型患者会进展为SPMS,表现为持续神经功能恶化。

迄今为止,已开发出多种免疫调节药物用于MS治疗,这些传统疗法虽可缓解症状,却难以实现髓鞘再生与神经修复,临床亟需新型干预策略。MSC凭借免疫调节、神经保护与自我更新特性,成为MS治疗潜力候选方案。
本研究是一项I/II期、单臂、开放标签临床研究,旨在通过评估神经系统、心理和免疫调节参数,探讨非冷冻保存、体外扩增的自体AT-MSC在SPMS患者中的安全性和临床疗效。
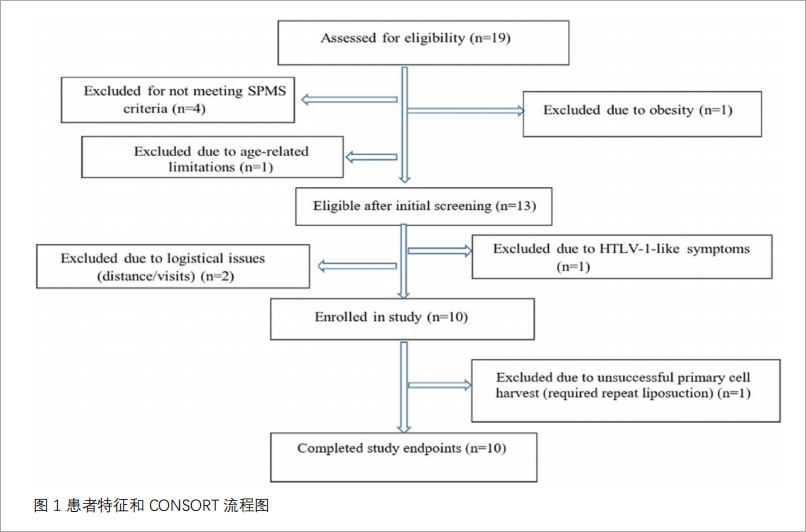
患者筛选:共纳入10名女性SPMS患者(图1),年龄26-49.6岁,平均病程10.8年,扩展残疾状态量表(EDSS)评分为4-6分、近1年EDSS进展≥0.5分、常规治疗效果不佳,排除感染、恶性肿瘤、妊娠及免疫抑制治疗者。
方 法:术前予氢化可的松与地塞米松预防过敏及免疫反应,采用高剂量静脉输注,平均总量245×10⁶个细胞/人(4.4×10⁶/kg),AT-MSC分两疗程,每次输注后,患者均需住院8小时,以监测生命体征和不良事件。
安全性数据:9个月随访期内主要不良事件为短暂发热、头痛、肌肉痉挛、轻度眩晕等,多在24小时内自行缓解;抽脂相关局部疼痛一周内改善,无感染、过敏、肝肾功能损伤及神经功能恶化,未出现严重不良事件。
功能改善情况:基线时所有患者均存在锥体束、感觉、肠道及膀胱功能障碍。移植后,2例患者斜视减轻、书写图形能力提升;6周时全部患者疲劳缓解、精力改善,3例肌力增强;自首次输注1周至研究终点,所有患者尿频、尿失禁等尿功能指标持续改善。
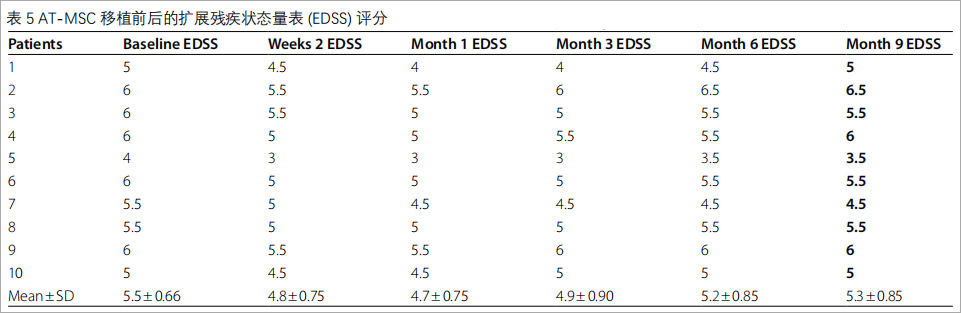
EDSS评分变化:基线平均EDSS为5.5分(表5),治疗后1个月降至4.7分,3个月时平均EDSS较基线下降0.6分,9个月时仍低于基线水平。整体呈现早期改善、中期稳定趋势,30%患者9个月内无疾病进展,证实干细胞对残疾进展的控制作用。
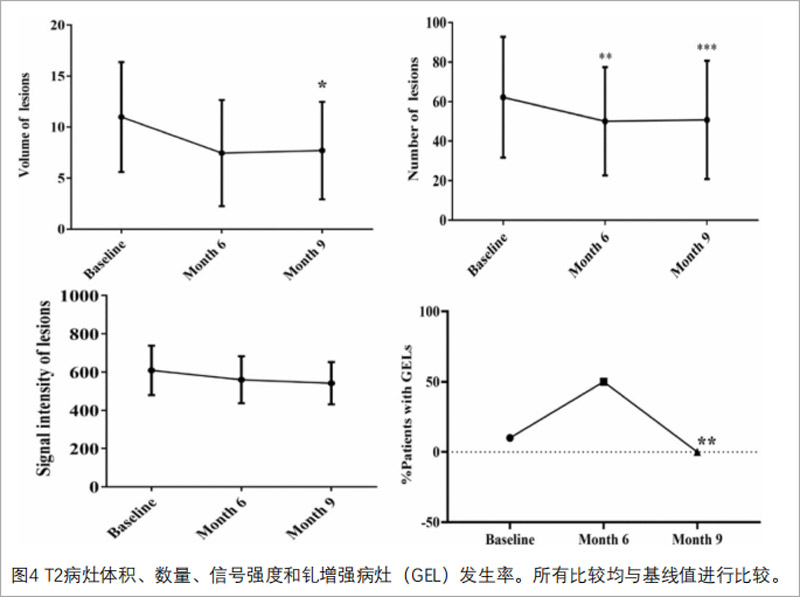
脑部MRI改善情况:T2-FLAIR病灶数量从基线至9个月持续显著减少(图4),病灶体积在6-9个月明显下降;钆增强病灶(GELs)在6个月时短暂升高后逐渐显著消退,提示治疗可减轻炎症活动、促进病灶修复,与临床功能改善形成对应。
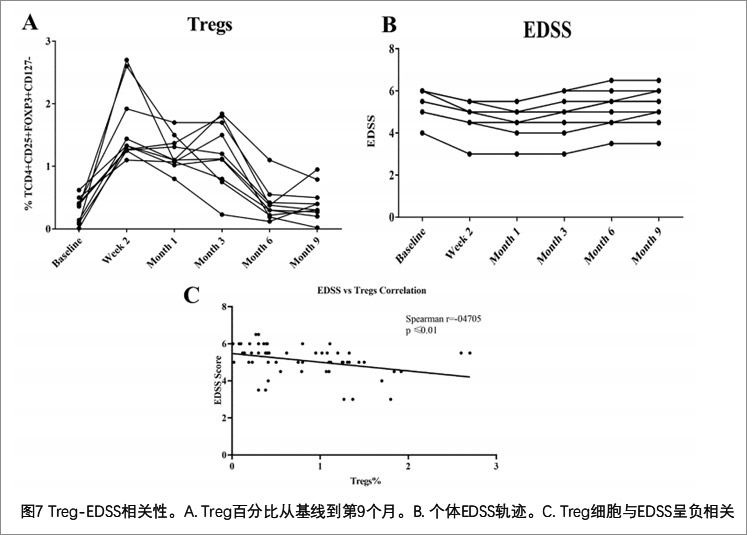
免疫调控:输注后2周到1个月Treg显著升高,3个月达峰值,9个月仍高于基线。同时抗炎因子TGFβ、IL-4、IL-10 与 FOXP3表达上调,促炎因子IL-1、IL-6、IL-17、IFN-γ显著下调,呈现强效免疫平衡效应。
进一步分析显示(图7),Treg比例与EDSS评分呈显著负相关,提示免疫调节是功能改善的关键机制。治疗早期以抗炎与免疫调控为主,后期伴随病灶修复与神经保护,形成“先控炎、后修复”的双重作用模式,与多数MSC治疗神经疾病的时序特征一致。
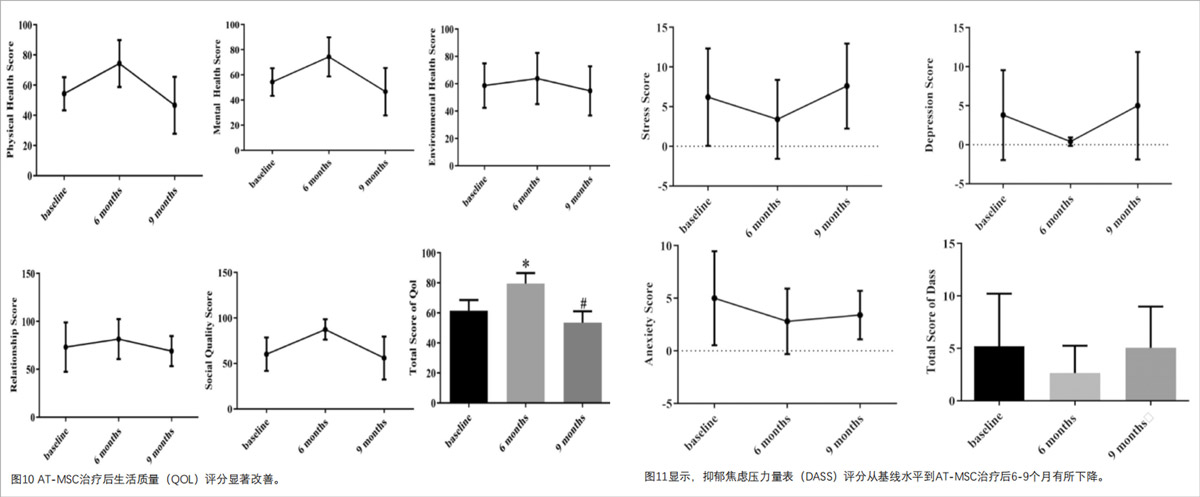
心理与生活质量:治疗后6个月与9个月,患者生活质量评分持续提升(图10),抑郁、焦虑、压力量表(DASS)呈下降趋势(图11)。同时疲劳感减轻、精力提升,尿功能明显改善,部分患者肢体力量增强,整体功能与身心状态全面优化。
本研究存在样本量偏小、无安慰剂对照、单臂设计等局限,需更大规模随机对照试验验证这一结果。但作为I/IIa期试验,已提供清晰安全性信号与积极疗效信号,为后续优化剂量、输注次数与给药途径奠定基础。
综上所述,高剂量自体AT-MSC治疗SPMS,安全性与耐受性良好,可显著降低EDSS评分、减少MRI病灶、增强免疫调节、改善生活质量。该疗法突破传统治疗局限,为SPMS提供兼具免疫调控与神经修复的再生策略。
未来应开展随机、双盲、安慰剂大规模对照试验,确定最佳剂量与疗程,延长随访时间,验证长期疗效与安全性,推动干细胞技术向临床转化,惠及更多进展型多发性硬化症患者。
参考资料:
Fahimeh Lavi Arab et al.Safety and feasibility of intravenous fresh adipose-derived mesenchymal stem cells in secondary progressive multiple sclerosis: phase I/IIa clinical results.Arab et al. Stem Cell Research & Therapy (2026) 17:120 10.1186/s13287-026-04933-6.